![]() Шановні колеги, вітаю Вас! Науковий семінар Інституту біохімії ім. О.В.Палладіна НАН України «Актуальні проблеми сучасної біохімії» продовжує свою роботу. 13 грудня 2016 р. (вівторок) о 10-30 в Актовій залі Інституту будемо слухати спільну доповідь проф. А.І. Соловйова (ДУ «Інститут фармакології та токсикології НАМН України») та проф. О.В. Жолоса («Інститут біології та медицини» Київського національного університету імені Тараса Шевченка, Інститут фізіології ім. О.О. Богомольця НАН України) «Наноструктуровані матеріали як модулятори активності іонних каналів: міфи і реалії». Авторські тези доповіді додаються. Запрошуємо Вас та Ваших колег до участі у роботі нашого семінару.
Шановні колеги, вітаю Вас! Науковий семінар Інституту біохімії ім. О.В.Палладіна НАН України «Актуальні проблеми сучасної біохімії» продовжує свою роботу. 13 грудня 2016 р. (вівторок) о 10-30 в Актовій залі Інституту будемо слухати спільну доповідь проф. А.І. Соловйова (ДУ «Інститут фармакології та токсикології НАМН України») та проф. О.В. Жолоса («Інститут біології та медицини» Київського національного університету імені Тараса Шевченка, Інститут фізіології ім. О.О. Богомольця НАН України) «Наноструктуровані матеріали як модулятори активності іонних каналів: міфи і реалії». Авторські тези доповіді додаються. Запрошуємо Вас та Ваших колег до участі у роботі нашого семінару.
З повагою – С.О.Костерін.
Наноструктуровані матеріали як модулятори активності іонних каналів: міфи і реалії
Проф. А.І. Соловйов
ДУ «Інститут фармакології та токсикології НАМН України»
Проф. О.В. Жолос
Інститут біології та медицини, Київський національний університет імені Тараса Шевченка
Інститут фізіології ім. О.О. Богомольця НАН України
 Іонні канали – це вбудовані в плазматичну мембрану клітини або в мембрани внутрішньоклітинних органел білкові структури, які контролюють надходження та вихід іонів, тим самим забезпечуючи регуляцію різних біологічних функцій, починаючи від контролю збудливості клітин і закінчуючи їх проліферацією та апоптозом. Іонні канали експресуються у всіх клітинах, де вони виконують різноманітні життєво важливі функції, тому не дивно, що з дефектами функціонування іонних каналів пов’язано ряд захворювань. Термін «каналопатія» визначає захворювання, які пов'язані з дисфункцією певного типу іонних каналів. До каналопатій відносять такі хвороби, як епілепсія, серцева аритмія, артеріальна гіпертонія, цукровий діабет та рак.
Іонні канали – це вбудовані в плазматичну мембрану клітини або в мембрани внутрішньоклітинних органел білкові структури, які контролюють надходження та вихід іонів, тим самим забезпечуючи регуляцію різних біологічних функцій, починаючи від контролю збудливості клітин і закінчуючи їх проліферацією та апоптозом. Іонні канали експресуються у всіх клітинах, де вони виконують різноманітні життєво важливі функції, тому не дивно, що з дефектами функціонування іонних каналів пов’язано ряд захворювань. Термін «каналопатія» визначає захворювання, які пов'язані з дисфункцією певного типу іонних каналів. До каналопатій відносять такі хвороби, як епілепсія, серцева аритмія, артеріальна гіпертонія, цукровий діабет та рак.
Калієві канали широко експресуються в різних типах клітин і, зокрема в гладеньком’язових. Забезпечуючи вихід калію з клітини назовні, їх активація призводить до гіперполяризації мембрани та розслаблення гладенького м’язу. Серед різних класів калієвих каналів, найбільш значущими в гладеньких м’язах є потенціал- та кальцій-залежні канали великої провідності (ВКСа). В найбільшому ступені вихід калію з міоцитів судин забезпечується саме ВКСа каналами, які мають подвійну природу активації – як зміщенням мембранного потенціалу в сторону деполяризації, так і за рахунок підвищення внутрішньоклітинного кальцію. Не зважаючи на значну роль цих каналів у регуляції судинного тонусу, на сьогоднішній день практично не існує ефективних фармакологічних засобів корекції їх функції, хоча фармацевтична промисловість протягом останніх двох десятиріч вела інтенсивний пошук препаратів для лікування різних захворювань (зокрема легенева гіпертензія, еректильна дисфункція, нестабільний сечовий міхур, біль при запаленні, бронхіальна астма) на основі природних та синтетичних активаторів ВКСа каналів. Основними проблемами залишаються низька селективність та ефективність цих препаратів (Nardi A., Olesen S.-P. (2008). BK channel modulators: a comprehensive overview. Curr. Med. Chem. 15, 1126–1146).
Ми пропонуємо принципово новий підхід для корекції дисфункцій іонних каналів, який змінює основну парадигму фармакології, за допомогою останніх досягнень в області нанотехнологій. Поєднання нано- та фотонних впливів в єдиний підхід створює унікальну синергію і відкриває перспективний шлях в напрямку принципово нових технологічних можливостей.
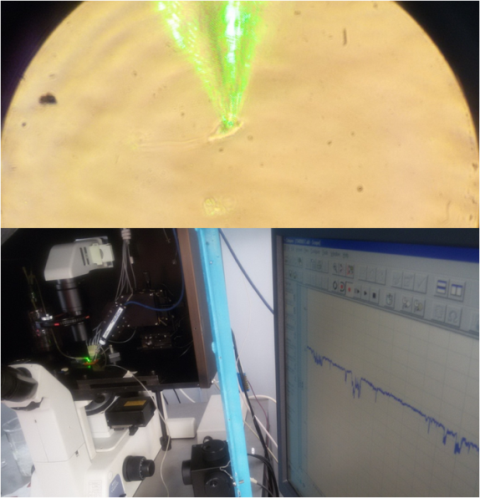
Були синтезовані колоїдні наночастинки золота з середніми розмірами 5 нм. Розчин концентрацією 10-3 М містив в собі 6.02 х 1020 наночастинок. Цим наночастинкам, як і більшості інших металів, притаманне явище плазмону – колективної осциляції хмари вільних електронів. Якщо плазмонна частинка набагато менша за довжину світла, то електромагнітне поле цього пучка світла викликає підсилення коливань електронної хмари – відбувається явище поверхневого плазмонного резонансу. Максимум поглинання наночастинок золота становить 510-570 нм, а отже плазмонний резонанс викликали за допомогою лазерного випромінювання з довжиною хвилі 532 нм і потужністю 5 мВт.
Ми показали, що плазмонні наночастинки золота в концентрації 10-5-10-4 М викликали розслаблення попередньо скорочених норадреналіном (10-6 М) гладеньком’язових препаратів аорти та легеневої артерії, і цей ефект підсилювався після опромінення препарату лазером.
До того ж, ми продемонстрували, що наночастинки в концентрації 10-4 М викликали збільшення вихідних калієвих струмів через ВКСа канали гладеньком’язових клітин аорти та легеневих артерій, а опромінення зеленим лазером достовірно підсилювало їх дію.
Також аналогічним чином збільшувалась вірогідність відкритого стану та кількість відкритих поодиноких калієвих каналів в міоцитах аорти, легеневих артерій та тонкого кишечнику. Такі результати наводять на думку дистанційного непрямого контролю, оскільки при реєстрації струмів в режимі cell-attached мембрана клітини не проривається, а зовнішній розчин з наночастинками не може потрапити безпосередньо до фрагменту мембрани, від якого реєструється активність калієвих каналів.
Отже, плазмонні наночастинки золота виявляють себе як активатори кальцій-залежних калієвих каналів в гладеньком’язових клітинах і в перспективі можуть бути застосовані у якості принципово нового фармакологічного препарату для корекції патології судин та інших органів, які пов’язані з дисфункцією калієвих каналів.
В доповіді також планується торкнутись теми впливу на гладеньком’язові клітини інших наноструктур - фулеренів С60, ліпосом та малих інтерферуючих РНК.

